Originally published in Compendium, an AEGIS Publications Property. All rights reserved.
Effects of Occlusion on Periodontal Wound Healing by Ann M. Decker, DMD; and Hom-Lay Wang, DDS, MSD, PhD. Originally published in Compendium of Continuing Education in Dentistry 39(9) October 2018. © 2018 AEGIS Publications, LLC. All rights reserved. Reprinted with permission of the publishers.
Despre autori:
Ann M. Decker, DMD
Department of Periodontics and Oral Medicine, University of Michigan School of Dentistry, Ann Arbor, Michigan; Periodontal Resident, PhD candidate, Graduate Periodontics, Department of Periodontics and Oral Medicine, University of Michigan School of Dentistry, Ann Arbor, Michigan
Hom-Lay Wang, DDS, MSD, PhD
Professor and Director of Graduate Periodontics, Department of Periodontics and Oral Medicine, University of Michigan School of Dentistry, Ann Arbor, Michigan
Obiective studiate:
- descrierea semnelor clinice şi a efectelor biologice ale ocluziei traumatice;
- enumerarea etapelor biologice ale vindecării plăgii după chirurgia parodontală;
- dezbaterea efectelor ocluziei asupra vindecării plăgii după chirurgia parodontală.
Trauma cauzată de ocluzie rămâne un concept importat în stomatologie. Ocluzia traumatică afectează sistemul biologic printr-o serie de evenimente care induc un răspuns inflamator aseptic şi resorbţie osoasă. Dovada clinică a acestor evenimente biologice este prezentă sub forma leziunilor traumatice sau a mecanismelor adaptative. Dacă aceste semne clinice nu sunt identificate înainte de chirurgia parodontală, poate rezulta eşuarea procedurii din cauza unei prezenţe exacerbate a leucocitelor şi a plăgii care nu se vindecă. Cu toate acestea, dacă trauma ocluzală este ajustată, dovezile demonstrează că pot avea succes până şi evenimentele inflamatorii majore, cum ar fi replantarea unui dinte avulsionat. Prin urmare, armonia contactelor ocluzale cu lipsa interferenţelor este esenţială pentru obţinerea regenerării parodontale/ regenerării osoase implantare predictibile.
Stresul mecanic survine la nivelul spaţiului ligamentelor parodontale (PDL) şi în regiunile localizate ale osului alveolar ca rezultat al ocluziei traumatice (de scurtă durată) sau al ortodonţiei (pe durate extinse). Aceste stresuri evocă un răspuns biochimic şi iniţiază o cascadă de evenimente biologice şi farmacologice. Când se aplică presiune la nivelul unei regiuni specifice, fluidul PDL este comprimat, osul alveolar se poate presa/plia, survin microdeplasări ale dintelui cu implicarea spaţiului PDL, celulele şi fibrele PDL se distorsionează, iar vasele sanguine se pot obtura parţial sau complet în funcţie de intensitatea forţei aplicate1.
În decursul câtorva minute în această situaţie, fluxul sanguin este modificat ducând la reducerea presiunii parţiale a oxigenului şi eliberarea primilor mesageri, a prostaglandinelor şi a citokinelor. Distorsiunea celulară şi hipoxia pot induce procesul cunoscut sub denumirea de inflamaţie aseptică, mediată de proteinele modelului molecular asociat distrugerii (damage-associated molecular pattern, DAMP)2.
Proteinele DAMP sunt factori endogeni care, în mod normal, sunt sechestraţi intracelular şi ascunşi de recunoaşterea sistemului imun în condiţii normale; cu toate acestea, în circumstanţele stresului/leziunii celulare, aceste molecule sunt eliberate în mediul extracelular, declanşând căi inflamatorii fiziologice, inclusiv calea prostaglandinelor şi a ciclooxigenazelor (COX)-1 şi COX-22. Dacă aceasta continuă timp de mai multe ore, modificările metabolice şi mesagerii secundari cum ar fi adenozin-monofosfatul ciclic pot regla în sus producţia citokinelor din cadrul superfamiliei factorului de necroză tumorală (TNF)-alpha care include activatorul receptorului pentru factorul de transcripţie nucleară [NF-κB] (RANK)/activatorul receptorului pentru ligandul NF-κB (RANKL şi moleculele sistemului osteoprotegerinei (OPG) stimulând remodelarea sau resorbţia osoasă2.
În cele din urmă, aceste procese biologice afectează activitatea chirurgilor dentari într-o varietate de moduri. Răspunsul inflamator provocat de proteinele DAMP eliberate de celulele distruse în punctul de dispersie a forţei ocluzale este procesat prin recrutarea de leucocite (precum neutrofile şi macrofage). Acest proces inflamator fiziologic este compus în timpul procedurilor chirurgicale parodontale, care iniţiază propria lor reacţie inflamatorie ce trebuie rezolvată.
Articolul de faţă încearcă să revizuiască efectele relevante biologice şi clinice ale forţelor ocluzale asupra structurilor parodontale şi vindecării plăgii.
EFECTELE ADVERSE ale ocluziei traumatice asupra rezultatelor clinice
Datorită acestor mecanisme biologice, ocluzia traumatică poate afecta advers rezultatele clinice şi vindecarea numeroaselor proceduri parodontale. Astfel, mobilitatea dentară şi ocluzia traumatică trebuie diagnosticate şi tratate timpuriu în procesul de planificare terapeutică. Discuţia privind complexitatea răspunsului la ocluzia traumatică în rândul pacienţilor are un istoric substanţial în sfera parodontologiei.
Reinhardt şi colab au utilizat analiza elementului finit pentru a încerca să înţeleagă în care anume punct o forţă aplicată la nivelul PDL poate iniţia o leziune (în cazurile de traumă primară şi secundară deopotrivă de origine ocluzală)3. Autorii au examinat în mod specific incisivii centrali maxilari. În mod interesant, reducerea înălţimii osului alveolar a avut efect minor asupra gradului de stres PDL până când reducţia osoasă a atins 6 mm (pierderea de suport osos de 60%), deşi valorile stresului se dublează la pierderile de os cuprinse între 4 şi 6 mm. Prin urmare, prognosticul unui dinte care a pierdut 4-6 mm din osul alveolar de susţinere este mai slab faţă de cel al omologului să din cauza cantităţii/agregării de forţe.
Mai mult, aceste rezultate sunt deosebit de relevante dacă în acest context urmează să fie finalizată o procedură de regenerare tisulară ghidată (guided tissue regeneration, GTR). Dacă forţe excesive se concentrează în punctul în care se încearcă regenerarea, procedura poate fi expusă riscului de eşec.
În plus, Harrel & Nunn au dezbătut efectele ajustării ocluzale asupra parodontitei4,5. Studiul lor a inclus 89 de pacienţi care prezentau boală parodontală şi înregistrări ocluzale la distanţe de peste 1 an. Pacienţii fie nu au primit niciun tratament (n=30), fie au beneficiat de detartraj nonchirurgical şi planare radiculară (n=18), fie au fost supuşi terapiei chirurgicale conform recomandărilor (n=41). Prima parte a rezultatelor din cadrul acestui studiu demonstrează că dinţii cu discrepanţe ocluzale iniţiale şi adâncimi de sondare iniţiale mai mari au un prognostic mai slab şi o mobilitate mai severă în comparaţie cu cei fără discrepanţe ocluzale4. Autorii au ajustat alţi factori de risc cunoscuţi ai bolii parodontale. Acest studiu furnizează dovada că discrepanţa ocluzală este un factor de risc independent care contribuie la boala parodontală.
Partea a II-a a rezultatelor studiului demonstrează că dinţii trataţi prin ajustare ocluzală (după necesităţi) sau dinţii fără discrepanţă ocluzală iniţială aveau o probabilitate de numai 60% de a manifesta agravarea condiţiei clinice globale, în comparaţie cu dinţii cu discrepanţă ocluzală care nu au beneficiat de tratament5. Autorii au dovedit că dinţii cu discrepanţă ocluzală care nu au fost trataţi niciodată au prezentat o creştere anuală semnificativ mai mare a adâncimii de sondare (periodontal probing, PD) decât dinţii care manifestau discrepanţe ocluzale iniţiale şi ajustări ocluzale sau care nu aveau discrepanţe ocluzale iniţiale. Deci, ocluzia traumatică poate afecta mobilitatea dentară şi adâncimile de sondare parodontală PD şi, ca atare, sănătatea parodontală.
Palcanis a studiat şi raportat la rândul său modificările fiziologice directe ale PDL, efectuând experimente pe un model canin şi urmărind să răspundă întrebărilor legate de modificările PDL în condiţiile traumei ocluzale6. S-a secţionat porţiunea coronară a dintelui, ceea ce a permis introducerea unei canule etanşe în spaţiul PDL dinspre spaţiul pulpar. Acesta a fost un model experimental unic care a permis menţinerea unui spaţiu fiziologic şi izolat pentru măsurătorile de presiune.
În plus, Biancu, Ericsson & Lindhe au încercat să înţeleagă ce modificări tisulare pot surveni în zona de co-distrugere pentru a determina de ce trauma poate induce pierderea adiţională de ataşament şi, de asemenea, dacă schimbările apar la nivelul ţesutului PDL atunci când o leziune inflamatorie se aproprie de spaţiul PDL7. Astfel, grupul de studiu era interesat de examinarea efectelor biologice ale ocluziei traumatice asupra spaţiului PDL.
Autorii au finalizat acest studiu pe câini din rasa beagle cu vârsta de 1 an. Opt câini au fost supuşi deplasărilor oro-vestibulare pentru a creşte mobilitatea dentară prin utilizarea elasticelor ortodontice poziţionate pe suprafeţele vestibulare ale coroanei dintelui testat. Elasticul a fost schimbat fie în poziţie bucală, fie în poziţie linguală de două ori pe săptămână, timp de 3 luni. Controlul plăcii s-a realizat până la finalul experimentului (ziua 90).
Rezultatele histologice din cadrul acestui experiment au demonstrat că în cea mai coronară porţiune a PDL la dinţii care manifestau mobilitate crescută, se observa o lăţime amplificată, o cantitate diminuată de colagen în spaţiul PDL şi un număr mai mare de structuri vasculare şi o cantitate mai mare de infiltrat inflamator (leukocite). În mod interesant, s-a remarcat şi o creştere a osteoclastelor la nivelul structurilor osoase alveolare adiacente şi reducerea numărului de fibre de colagen care se inserau pe cementul radicular/osul alveolar. Deci, se poate concluziona că trebuie depăşite (biologic şi fiziologic) modificările calitative în parodonţiul asociat forţelor excesive care au dus la o mobilitate dentară accentuată în scopul de a minimiza distrugerea colaterală şi pentru a obţine vindecarea plăgii.
De asemenea, un grup brazilian a publicat un studiu cu utilizarea unui model de şobolan cu restaurări elevate, din amalgam sau compozit, pentru a examina efectele traumei ocluzale asupra PDL8. Rezultatele histologice au demonstrat că efectele traumatice (adică PDL cu aspect dezorganizat şi suprafeţele alveolare demonstrând mai multe neregularităţi) asupra dinţilor restauraţi cu amalgam au fost mai extinse decât în cazul celor restauraţi cu răşini compozite.
SEMNELE TRAUMEI DE CAUZĂ OCLUZALĂ
Trauma de origine ocluzală (trauma from occlusion, TFO) este reprezentată de dezvoltarea modificărilor patologice ca un rezultat al forţei excesive, produsă de muşchii masticatori. Poate exista în contextul obiceiurilor parafuncţionale, în situaţii iatrogenice, în malocluzie sau migraţii dentare. Stillman a definit în continuare acest termen ca “o condiţie în care leziunea survine la nivelul structurilor de susţinere a dinţilor prin acţiunea de aducere a maxilarelor într-o poziţie închisă.”9 Cauzele TFO pot include contactele premature, parafuncţia (bruxismul) şi modificarea poziţiei dentare de-a lungul timpului.10
Mai mult, glosarul de termeni emis de Academia Americană de Parodontologie defineşte subclasa de traumă ocluzală primară ca fiind o leziune determinată de forţele ocluzale excesive aplicate pe un dinte sau pe dinţi cu suport normal, în timp ce trauma ocluzală secundară este definită ca leziunea indusă de forţele ocluzale normale aplicate pe un dinte sau pe dinţii cu suport parodontal inadecvat.11 Trauma ocluzală combinată se referă la leziunea rezultată de pe urma forţelor ocluzale anormale aplicate pe un dinte cu suport parodontal inadecvat.12 În fine, ocluzia traumatică este definită ca orice ocluzie care produce forţe ce cauzează o leziune la nivelul aparatului de ataşament.11
Semnele clinice ale ocluziei asupra parodonţiului pot varia în rândul indivizilor. Jin & Cao au realizat un studiu pentru a determina fiabilitatea semnelor selectate ale TFO şi relaţia lor cu severitatea parodontitei, cu utilizarea a 32 pacienţi cu parodontită cronică moderată spre avansată din cadrul Universităţii Medicale din Beijing.13 Toţi dinţii prezenţi au fost evaluaţi în privinţa contactelor ocluzale anormale, a semnelor de TFO şi severitatea parodontitei.
Autorii au identificat factorii care separau dinţii ce manifestau dovezi de distrugere traumatică (ex. valori PD crescute, pierdere osoasă, etc.) de dinţii care se adaptaseră la forţe şi care au rămas “stabili” (ex. pierdere mai mică de ataşament clinic [clinical attachment loss CAL], înălţime osoasă mai mare). Autorii au segmentat aceşti dinţi în două categorii: trauma pe baza indicelui de ocluzie (trauma from occlusion index, TOI) şi indicele de adaptabilitate (adaptability index, AI).
Grupul TOI se caracteriza prin PDL lărgit şi mobilitate funcţională (fremitus) şi era susceptibil la TFO cu valori de sondare PD şi CAL crescute şi înălţimi osoase diminuate. Grupul AI se caracteriza prin faţete de uzură şi lamina dura îngroşată şi era mai rezistent la TFO cu valori CAL mai mici, alături de o înălţime osoasă mai mare.
LIPSA OCLUZIEI
După cum s-a observat anterior, încărcarea mecanică iniţiază în mod direct procesul de remodelare osoasă; cu toate acestea, hipofuncţia ocluzală cauzată de pierderea unui dinte antagonist iniţiază osteoporoza de neutilizare.14 În mod interesant, mecanismele care ghidează pierderea osului nu sunt bine elucidate.
Xu şi colab au raportat recent că hipofuncţia ocluzală duce la pierderea osului şi deteriorarea arhitecturii corelată cu suprareglarea moleculei secretate de osteoclaste sclerostin (osteocyte-secreted molecule sclerostin, SOST), care la rândul său antagonizează calea de semnalizare Wnt/ß-catenină prin cuplarea la receptorul LRP5/6 pentru a inhiba formarea osului de către osteoblaste.15
Mai mult, suprareglarea SOST induce activitate osteoresorbtivă prin promovarea osteoclastogenezei şi expresia RANKL. Sunt necesare studii viitoare care să utilizeze modele de hipo-ocluzie pentru a elucida complet mecanismele care guvernează aceste evenimente biologice.
FAZELE VINDECĂRII PLĂGII PARODONTALE
Vindecarea plăgii este o componentă esenţială în domeniul chirurgiei parodontale şi poate fi influenţată de efectele ocluziei. Aşa cum se afirma anterior, sunt implicate stadii multiple în dobândirea rezoluţiei şi a homeostaziei biologice atât în cazul ocluziei traumatice, cât şi al chirurgiei parodontale. În cele ce urmează este prezentată o analiză concisă a acestor etape:
Hemostaza şi faza de inflamaţie
Obiectivele clinice primare are hemostazei şi ale fazei inflamatorii din cadrul vindecării plăgii parodontale constau în eliminarea bacteriilor sau a altor antigeni şi obţinerea coagulării primare/suportului la nivelul regiunii lezate. În cursul hemostazei, fibrinogenul din exsudat iniţiază mecanismul de coagulare şi creează o reţea bogată în fibrină, determinând oprirea sângerării.16 De la primele minute şi până la 24 de ore, răspunsul inflamator este în plin efect, implicând răspunsuri celulare şi vasculare deopotrivă. Eliberarea de histamină şi serotonină la nivelul regiunii cauzează vasodilataţie şi permite fagocitelor să traverseze în plagă.16
Neutrofilele sunt atrase de chemokine, cascada complementului şi peptidele eliberate în cursul scindării fibrinogenului în cadrul cascadei de coagulare.17 Odată ajunse în plagă, neutrofilele încearcă să cureţe plaga prin eliberarea de specii de oxigen reactive, eliberare de proteaze care lizează celulele bacteriene din regiune, îndepărtarea resturilor prin fagocitoză şi formarea de capcane extracelulare neutrofile (neutrophil extracellular traps, NET).18
NEToza este procesul prin care neutrofilele sunt supuse întreruperii membranei nucleare şi granulare, decondensării de cromatină, difuziune în citoplasmă şi amestecarea proteinelor citoplasmatice.19,20 Aceasta este urmată de ruptura membranei plasmatice şi de eliberarea fibrelor de cromatină formate din ADN, histone şi 20 proteine diferite, incluzând elastaza, mieloperoxidaza, catepsina G, proteinaza 3, proteina B1 din grupul cu înaltă mobilitate şi LL37.18 NEToza duce la activarea celulelor imune care pot da naştere la NEToză suplimentară, oferind o barieră mai mare împotriva avansării antigenilor microbieni.
În acest scop, capcanele NET agregate se sechestrează în cele din urmă şi degradează mediatorii proinflamatori în încercarea de a abroga inflamaţia excesivă/cronică. Dacă NEToza nu se rezolvă prin aceste mecanisme, se poate dezvolta plaga cronică şi lipsită de vindecare.18 Recent bolile autoimune şi stările inflamatorii cronice (ex. artrita reumatoidă, lupusul sistemic eritematos şi ulcerele diabetice) au fost asociate cu mecanismele de NEToză nerezolvate.21
În plus, macrofagele sunt de asemenea un regulator imunologic esenţial al debridării plăgii localizate şi al rezoluţiei inflamaţiei.22 Macrofagele M1, în rândul cărora există numeroase subtipuri, au o prezenţă crescută în cursul fazei inflamatorii şi fenotipurile M2a se pot supraregla ulterior într-un fenotip antiinflamator pentru a ajuta iniţierea rezoluţiei inflamatorii a plăgii şi a vindecării.23 Ca răspuns la stimulii microbieni (ex. lipopolizaharide) sau citokine (TNF şi factor de stimulare a coloniilor de granulocite macrofage [GM-CSF]), poate fi favorizată polarizarea macrofagelor M1 activate clasic.24 Similar, alte citokine (ex. interleukina [IL]-4, IL-13, IL-33) sunt asociate cu polarizarea macrofagelor alveolare la un fenotip M2.24
Faza de migraţie
Faza migratorie din cadrul vindecării ţesutului epitelial se numeşte astfel datorită deplasării celulelor epiteliale şi a fibroblastelor, care progresează dinspre marginile leziunii, dezvoltându-se rapid deasupra leziunii tisulare şi sub crustă. Această migraţie celulară este un pas esenţial în înlocuirea ţesutului pierdut şi este ghidată de interacţiunile intercelulare şi factorii locali.25
Faza proliferativă
Faza proliferativă survine în conjuncţie şi după faza migratorie (cam din ziua 3+). În acest moment, ţesutul de granulaţie s-a format prin creşterea spre interior a vaselor capilare şi limfatice, către zona lezată. Colagenul este sintetizat de fibroblaste, asigurând regiunii formă şi rezistenţă, în mod continuu, timp de 14 zile. Finalul acestui stadiu este marcat de o diminuare a densităţii vasculare şi de edem.26
Faza de remodelare
Această fază este caracterizată prin maturarea ţesutului conjunctiv celular şi îngroşarea accentuată a epiteliului care va duce în cele din urmă la prezentarea cicatricii finale. În mod interesant, ţesutul de granulaţie celulară este modificat biologic într-o masă acelulară în decursul unei perioade de câteva luni şi până la 2 ani.27
EFECTELE OCLUZIEI ASUPRA VINDECĂRII PLĂGII PARODONTALE
Vindecarea plăgii trebuie să progreseze printr-o serie de etape, incluzând răspunsul şi rezoluţia inflamatorie şi remodelarea şi maturarea finală a structurii. Tabelul 1 oferă un rezumat al efectelor traumei ocluzale asupra parodonţiului, inclusiv consecinţele biologice, semnele clinice şi efectele asupra rezultatelor clinice.
Când se urmăreşte vindecarea plăgii în zona PDL, trauma ocluzală trebuie luată în considerare din perspective biologice şi fiziologice deopotrivă, pentru că ea poate cauza modificări nedorite la locul vindecării şi inhibarea nedorită a creşterii osoase susţinute. Mai exact, ocluzia traumatică poate cauza dezorientarea fibrelor PDL, o diminuare a cantităţii fibrelor de colagen, creşterea infiltratului de celule imune, o deplasare a balanţei de remodelare osoasă spre osteoclastogeneză, tromboză venoasă şi necroza celulelor PDL, aşa cum descria recenzia de mai sus a literaturii.
În plus, ocluzia poate influenţa reparaţia PDL şi aprovizionarea neurovasculară a pulpei.28 Toate aceste efecte ale traumei ocluzale laolaltă sunt amplificate în contextul unei situaţii de reparaţie a plăgii, cum ar fi plasarea unui implant, GTR sau în cazul unor dinţi subluxaţi. Figura 1 ilustrează un rezumat al efectelor ocluziei asupra vindecării plăgii.
Este în beneficiul pacientului parodontal să se verifice contactele şi excursiile ocluzale în contextul unei proceduri chirurgicale sau regeneratoare într-o anumită regiune, îndeosebi dacă există o restaurare în zona respectivă, astfel încât să se poată obţine rezoluţia inflamatorie, cu permiterea timpului maxim pentru regenerare şi reparaţia ţesuturilor implicate.
De asemenea, în pofida indicaţiilor potrivit cărora pierderea osului cauzată de ocluzia traumatică este reversibilă în absenţa inflamaţiei induse de placă, dovezile au stabilit că o plagă dintr-o locaţie aflată în ocluzie traumatică poate împiedica reparaţia PDL şi a regresiei resorbţiei osoase, ceea ce este contraproductiv în contextul regenerării şi vindecării plăgii într-o regiune parodontală.28 Astfel, practicienii dentari ar trebui să fie atenţi la evaluarea ocluzală pentru a asigura faptul că nu există TFO, îndeosebi atunci când se încearcă proceduri GTR. Armonia contactelor ocluzale fără interferenţe este necesară pentru a obţine regenerarea parodontală/osoasă implantară predictibilă.
IMPLICAŢII CLINICE ŞI CONCLUZII
Pe baza datelor disponibile, autorii concluzionează că ocluzia traumatică poate stimula un efect inflamator dăunător, similar cu plăgile cronice, care în cele din urmă poate afecta regenerarea ţesuturilor locale. În plus, stările inflamatorii cronice ale plăgilor cauzate de încărcarea ocluzală pot fi exacerbate în contextul tulburărilor autoimune sau al condiţiilor inflamatorii cronice (ex. diabet) şi ar trebui luate măsuri pentru a atenua trauma, în special în asemenea cazuri.
În fine, toate cele patru stadii ale vindecării plăgii – hemostaza şi inflamaţia, migraţia, proliferarea şi remodelarea – sunt componente esenţiale ale procesului de vindecare a plăgii, iar existenţa prelungită în oricare dintre aceste stări poate fi dăunătoare pentru rezultatul regenerator final.
Astfel, implicaţiile clinice pentru regenerarea ţesuturilor în prezenţa traumei ocluzale includ îndepărtarea tuturor interferenţelor (axiale şi non-axiale) care cauzează sau generează orice grad de fremitus. Important este de reţinut că interferenţele ocluzale (de partea lucrătoare şi nelucrătoare) ar trebui evaluate şi ajustate înainte de administrarea anesteziei locale a regiunii pentru a asigura observarea schemelor ocluzale fiziologice în condiţii normale proprioceptive. De asemenea, examinarea specifică a fremitusului ar trebui evaluată şi cu ocazia tuturor şedinţelor postoperatorii, pentru că ghidajul ocluzal se poate schimba în timp.
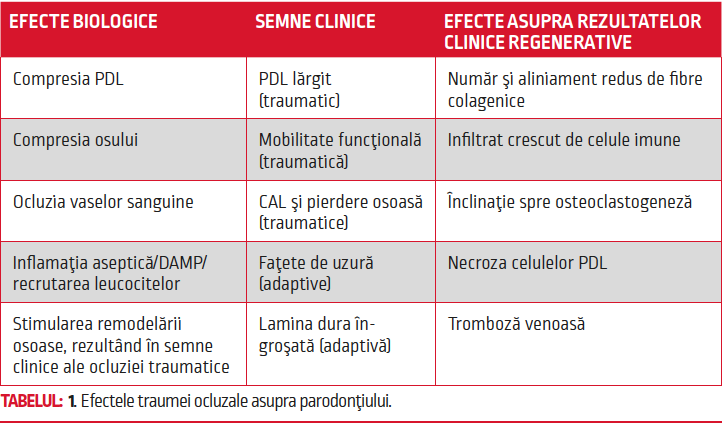
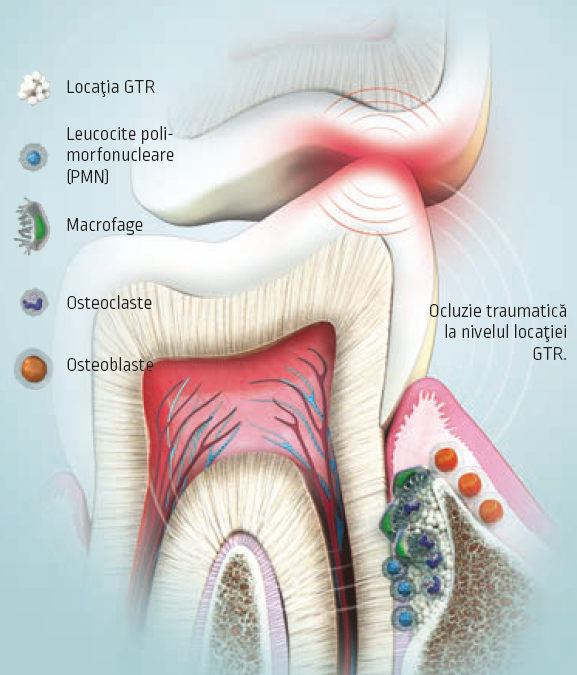
Fig. 1 Cascada vindecării plăgii în raport cu ocluzia. Efectele ocluziei traumatice sunt exacerbate în prezenţa chirurgiei parodontale cum ar fi regenerarea tisulară ghidată (GTR). Aceste efecte pot include compresia PDL, tromboza, infiltratul inflamator nerezolvat, amplificarea osteoclastogenezei şi eşuarea grefei. În acest scop se poate observa creşterea infiltraţiei limfocitare, alături de resorbţia osoasă, care contracarează răspunsul vindecării plăgii, necesar pentru rezoluţia procedurilor chirurgicale parodontale.
![]()
Verifică-ți cunoștințele acumulate după parcurgerea articolului prin rezolvarea CHESTIONARULUI următor:
1. Când se aplică presiune pe o anumită arie a spaţiului ligamentului parodontal (PDL) şi pe o regiune localizată a osului alveolar:
- a. fluidul PDL se deplasează liber;
- b. osul alveolar se poate presa/plia;
- c. celulele PDL şi fibrele sunt neafectate;
- d. vasele sangvine se menţin libere şi neblocate.
2. Răspunsul inflamator declanşat de proteinele DAMP eliberate din celulele distruse la nivelul punctului de dispersie a forţelor ocluzale se procesează prin:
- a. recrutarea leucocitelor;
- b. acumularea antigenelor patogene;
- c. alergenii din mediul oral;
- d. vindecarea plăgii.
3. Harrel & Nunn au demonstrat că dinţii cu discrepanţă ocluzală care nu au fost trataţi niciodată prezentau:
- a. sângerare crescută la sondare (BOP);
- b. pierdere redusă de ataşament clinic (CAL);
- c. valori crescute ale adâncimii de sondare (PD);
- d. pierdere osoasă redusă.
4. Biancu şi colab au demonstrat că cea mai coronară porţiune a PDL al dinţilor cu mobilitate amplificată din cauza ocluziei traumatice:
- a. avea o lăţime crescută;
- b. prezenta o cantitate crescută de colagen;
- c. avea mai puţine structuri vasculare;
- d. prezenta un infiltrat inflamator mai redus.
5. Trauma de ocluzie (TFO) reprezintă dezvoltarea modificărilor patologice ca rezultat al:
- a. factorilor endogeni sechestraţi intracelular;
- b. forţelor excesive produse de muşchii masticatori;
- c. mucozitei periimplantare;
- d. cariilor ocluzale.
6. Orice ocluzie care produce forţe ce cauzează o leziune la nivelul aparatului de ataşament este considerată:
- a. traumă ocluzală primară;
- b. traumă ocluzală secundară;
- c. traumă ocluzală combinată;
- d. ocluzie traumatică.
7. În studiul întreprins de Jon & Cao, grupul cu indicele de adaptabilitate (AI) era comparativ cu grupul traumei din indicele de ocluzie (TOI):
- a. mai puţin rezistent la TFO cu CAL mai mare;
- b. mai rezistent la TFO cu CAL mai redusă;
- c. mai rezistent la TFO cu CAL mai mare;
- d. la fel de rezistent la TFO, fără CAL.
8. Care fază a vindecării plăgii parodontale ţinteşte eliminarea bacteriilor şi obţinerea coagulării primare/a suportului pentru regiunea lezată?
- a. faza de hemostază şi inflamaţie;
- b. faza migratorie;
- c. faza proliferativă;
- d. faza de remodelare.
9. Colagenul este sintetizat de fibroblaste, care asigură formă şi rezistenţă continuă regiunii lezate timp de:
- a. 2 zile;
- b. 7 zile;
- c. 14 zile;
- d. 21 zile.
10. Armonia contactelor ocluzale fără interferenţe este necesară pentru a obţine în mod predictibil:
- a. hemostaza;
- b. prezenţa macrofagelor M1;
- c. regenerarea tisulară ghidată;
- d. regenerarea osului parodontal/implantar.
(răspunsuri corecte: 1b, 2a, 3c, 4a, 5b, 6d, 7b, 8a, 9c, 10d).
Referinţe bibliografice:
1. Krishnan V, Davidovitch Z. Cellular, molecular, and tissue-level reactions to orthodontic force. Am J Orthod Dentofacial Orthop. 2006;129(4):469.e1-e32.
2. Chen GY, Nuñez G. Sterile inflammation: sensing and reacting to damage. Nat Rev Immunol. 2010;10(12):826-837.
3. Reinhard RA, Pao YC, Krejci RF. Periodontal ligament stresses in the initiation of occlusal traumatism. J Periodontal Res. 1984;19(3):238-246.
4. Nunn ME, Harrel SK. The effect of occlusal discrepancies on periodontitis. I. Relationship of initial occlusal discrepancies to initial clinical parameters. J Periodontol. 2001;72(4):485-494.
5. Harrel SK, Nunn ME. The effect of occlusal discrepancies on periodontitis. II. Relationship of occlusal treatment to the progression of periodontal disease. J Periodontol. 2001;72(4):495-505.
6. Palcanis KG. Effect of occlusal trauma on interstitial pressure in the periodontal ligament. J Dent Res. 1973;52(5):903-910.
7. Biancu S, Ericsson I, Lindhe J. Periodontal ligament tissue reactions to trauma and gingival inflammation: an experimental study in the beagle dog. J Clin Periodontol.1995;22(10):772-779.
8. Jabôr GM, Suchard CA, Martins Filho CM, Tames DR. Effects of occlusal trauma on the periodontal ligament and alveolar bone of rat molars restored with composite resin and amalgam. Jornal Brasileiro de Oclusão, ATM e Dor Orofacial. 2003;3(10):153-157.
9. Stillman PR. The management of pyorrhea. Dental Cosmos. 1917;59
(4):405-414.
10. Lindhe J, Ericsson I. Trauma from occlusion: periodontal tissues. In: Lindhe J, Lang NP, eds. Clinical Periodontology and Implant Dentistry. 6th ed. Hoboken, NJ: John Wiley & Sons; 2015.
11. Glossary of Periodontal Terms. 4th ed. Chicago, IL: American Academy of Periodontology; 2001.
12. Bjorndahl O. Periodontal traumatism. J Periodontol.1958;29(3):223-231.
13. Jin LJ, Cao CF. Clinical diagnosis of trauma from occlusion and its relation with severity of periodontitis. J Clin Periodontol.1992;19(2):92-97.
14. Bikle DD, Halloran BP. The response of bone to unloading. J Bone Miner Metab. 1999;17(4):233-244.
15. Xu Y, Wang L, Sun Y, et al. Sclerostin is essential for alveolar bone loss in occlusal hypofunction. Exp Ther Med. 2016;11(5):1812-1818.
16. Boateng JS, Matthews KH, Stevens HN, Eccleston GM. Wound healing dressings and drug delivery systems: a review. J Pharm Sci. 2008;97(8):2892-2923.
17. Kolaczkowska E, Kubes P. Neutrophil recruitment and function in health and inflammation. Nat Rev Immunol. 2013;13(3):159-175.
18. Yang H, Biermann MH, Brauner JM, et al. New insights into neutrophil extracellular traps: mechanisms of formation and role in inflammation. Front Immunol. 2016;7:302.
19. Fuchs TA, Abed U, Goosmann C, et al. Novel cell death program leads to neutrophil extracellular traps. J Cell Biol. 2007;176(2):231-241.
20. Brinkmann V, Reichard U, Goosmann C, et al. Neutrophil extracellular traps kill bacteria. Science.



